Niti-S大腸用ステント多施設共同前向き安全性観察研究
プロトコール
Prospective Feasibility Study of D-Weave Uncovered Stent for Colon Protocol
大腸用ステントを用いた悪性結腸直腸閉塞の治療
Treatment of malignant colo-rectal obstruction with
Colonic Stent
結腸直腸の悪性閉塞に対する術前の処置および姑息的治療
Palliation and "Bridge to Surgery" endoscopic treatment of malignant stricture in the colon and rectum
大腸ステント安全手技研究会
平成25年7月29日作成 Ver.2
UMIN試験ID: UMIN000011304
目次
- 目的
- 研究の意義
- 対象機器
- 試験デザイン・研究対象症例数・参加施設・研究期間
- 対象集団
- 患者登録
- 患者フォローアップとエンドポイント
- データ解析
- 倫理規定
- データセンターについて
- 研究責任者と研究費について
- 研究問い合わせ窓口
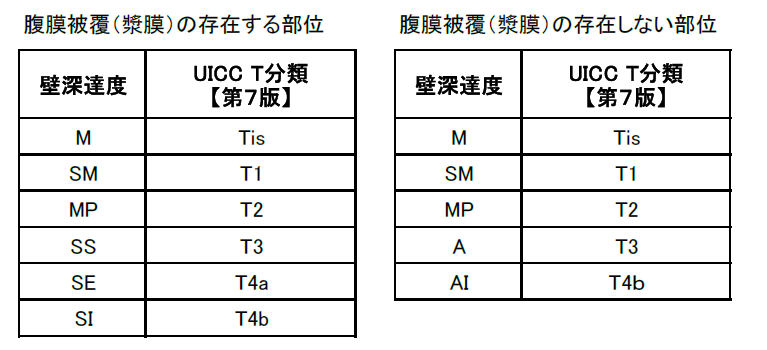
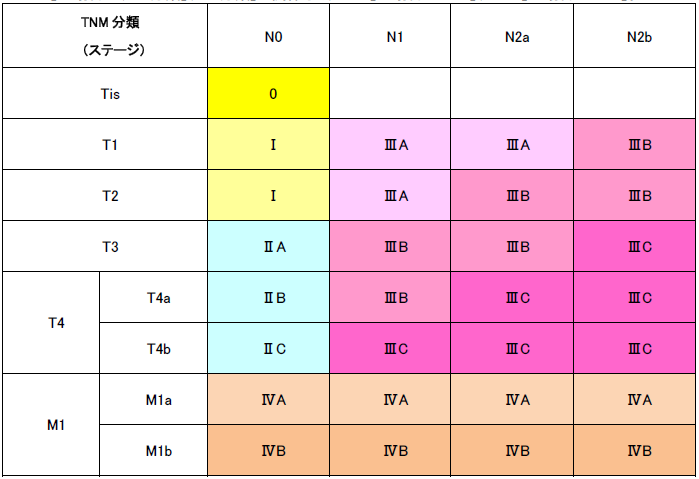
- 参考:大腸がんUICC-TNM第7版
本観察研究の目的は、悪性結腸直腸閉塞の治療における大腸用ステントである、Niti-S Colonic Stentの臨床使用経験を蓄積し、その有効性と安全性を評価する事である。研究に参加した医師または参加した施設の通常の治療方法を変更することが目的ではない。患者は通常の治療方法によって治療を受けることになる。また、通常大腸ステントは術前腸管減圧(Bridge to surgery: BTS)と根治切除不能例に対する緩和治療とに分けられるので、それぞれに検討する事とする。
The objective of this registry is to compile clinical experience of use of the Niti-S Enteral Colonic Stent for the treatment of malignant colo-rectal strictures. It is not the goal to change the usual treatment practice of the investigator or the center. Patients will be treated as per usual medical practices.
これまで、本邦では大腸狭窄に対する金属ステントは本邦で薬事認可も保険収載もなかったため、限られた施設での臨床研究として、食道用ステントの流用や、海外から大腸用ステントを個人輸入して手技が施行されてきた。しかし2011年7月にようやく米国製の大腸用ステントであるWallFlex Colonic Stentの薬事認可が承認され、2012年からは保険収載の上で使用可能となり、全国で急速に広まっている。
大腸ステント留置術については、今までの本邦の報告や欧米の報告では、技術的成功率が9割以上、臨床的成功率も約9割程度と良好な成績が報告されている。また留置手技に関する合併症も少なく、穿孔率が0-4%、合併症全体でも2-10%程度である。また、緩和治療目的の場合には長期の観察で1割程度の再閉塞、1割程度の逸脱、4%程度の穿孔率が報告されているが、患者のQOLの向上からみれば十分許容範囲内であると思われる。しかし一部では、緩和治療目的のrandomized clinical trial (以降RCT)で4割の穿孔率のため、前向きの研究が中止になった報告(van Hooft: Lancet. 2006)や、欧州での大腸癌イレウスに対する大腸ステント留置と緊急手術のRCTでもステント群での穿孔率(13%)の高さから研究の中断がなされており(Hooft JE, Lancet Oncol 2011)、大腸ステントの安全性については依然として疑問が持たれている。
我々は、本研究に先立ち、日本消化器内視鏡学会附置研究会である「大腸ステント安全手技研究会」のもと、東邦大学医療センター大橋病院が主任研究施設となり、全国の50施設が参加する多施設共同研究である、大腸ステント前向き安全性観察研究(UMIN000007953)を行い、WallFlex stentを用いた大腸ステント留置の安全手技を確立し、学会活動を通してその啓蒙を行ってきた。
今回、新たなステントである、Niti-S Enteral Colonic Uncovered Stent, D-typeが薬事認可された。本ステントに関する報告は、海外(Moon CM, Dis Colon Rectum 2010, Cheung DY, Surg Oncol 2012)や本邦(Tominaga K, Dis Colon Rectum 2012, Yoshida S, Dig Endosc 2013)で散見されるが、WallFlex Colonic Stentのような、単一のステントに関する大規模な症例での多施設にわたる有効性と安全性の評価は行われていない。本ステントに関する、全国的な大腸ステントの安全な手技の啓蒙を目指す事は、新たな安全に使用できる大腸ステントの選択肢を増やすだけでなく、本邦の大腸悪性狭窄患者のQOLの向上およびその安全性情報の世界へ向けた発信としても意義は大きい。
このため、新たに本ステントが保険収載されるにあたり、その有効性および安全性の本邦における評価が必要と考え、本研究を検討することとした。
なお本研究も、日本消化器内視鏡学会附置研究会である「大腸ステント安全手技研究会」のもと、東邦大学医療センター大橋病院が主任研究施設となり、全国の50施設が参加する多施設共同研究となる。
本品はナイチノール製ワイヤーを編み込んだ、自己拡張型金属ステントである。アキシャルフォースの低減を目的に、本品はステントの網目を独自のダイヤモンド構造としている。この網目構造及び原材料はNiti-S胃十二指腸用ステントと同一である。ステントにはステンレス鋼及びプラチナ/イリジウム合金製のX 線不透過マーカーがワイヤーの両端及び中央部に固定されている。ステントは予めデリバリーシステムに装填されており、自己拡張機能を有するステントが狭窄部に留置されることにより管腔を維持する。デリバリーシステムについても、Niti-S胃十二指腸用ステントと同一であり、インナーカテーテルは、中央に0.035インチのガイドワイヤーを通すルーメンがある。本品は内視鏡のワーキングチャンネル(最小チャンネル径:3.7 mm)を通して挿入することができる。デリバリーシステムにはアウターシース先端、ステント搭載時のステント両端および中央部の4ヶ所X線不透過マーカーが配置されている。
本品はMRIとの併用について、3テスラ以下のMRI環境下では、患者に対しリスクや有害事象の発生を増大させることはない。なお、ステントによって、磁場の歪みによるアーチファクトが生じる可能性があることに留意する必要がある。 本品はエチレンオキサイドガス処理によって滅菌された状態で供給されるが、高温、多湿、直射日光及び水濡れを避けて保管する必要がある。本品は一人の患者さんにのみ使用されるよう設計されている(Single use only)。
本観察研究は多施設共同で前向きな症例集積研究である。前向きな症例集積であり、安全性や有効性を評価するために一定の患者選択基準は設けるが、留置方法などについて規定するものではない。全国の病院から200症例のデータを蓄積することを目標とする。対象となる病院は、大腸ステント安全手技研究会の大腸ステント安全留置のためのミニガイドラインに従い本手技を安全に施行できると判断された、内視鏡治療の実績を高く評価されている施設である。
研究期間は、2013年10月11日から2015年10月10日までとする。
対象は大腸閉塞に対して大腸ステントを留置された症例で、200症例のデータ蓄積を目的とする。適応基準は製品の使用説明に従う。当該医師または当該施設の通常の治療方法を変更することが目的ではない。患者は通常の診療によって治療およびフォローアップを受けることになる。
- a. 適応 Indication
-
悪性新生物によって生じた結腸直腸閉塞の術前処置BTSおよび緩和治療を必要とする患者。
大腸用ステント留置術を受けたことのない患者のみが登録される。
Patients requiring palliative treatment of colorectal strictures produced by malignant neoplasms.
Only patients with no previous colonic stenting will be included in the registry.
-
悪性新生物によって生じた結腸直腸閉塞の術前処置BTSおよび緩和治療を必要とする患者。
- b. 禁忌 Contra-Indication
-
以下のいずれかを認める患者は登録できない。
- 腸虚血
- 穿孔の疑いまたは切迫
- 腹腔内膿瘍/穿孔
- 良性狭窄
- 内視鏡手技を適用できない患者
- 使用(登録)適応の項の具体的記述に該当しない使用法
- 患者が登録に同意しない場合
大腸用ステントは取扱説明書に従って使用する。
Patients contraindicated will include those presenting.- enteral ischemia
- suspected or impending perforation
- intrabdominal abscess / perforation
- benign strictures
- patients for whom endoscopic techniques are contraindicated
- any use other than those specifically outlined under indications of use (inclusion)
- in case that patient does not consent about registration
-
以下のいずれかを認める患者は登録できない。
-
大腸用ステントがすでに留置されている患者は、本研究に登録されない。
大腸用ステントは取扱説明書に従って使用する。
A patient with a previous colonic stent implanted will not be eligible to be introduced into the registry data base.
The Colonic Stent will be used in accordance to the instructions for use.
A patient with a previous colonic stent implanted will not be eligible to be introduced into the registry data base.
The Niti-STM Enteral Colonic Stent will be used in accordance to the instructions for use.
登録施設は、研究終了までの対象全例の登録を行うこととする。
登録時期は、施行前または施行後できるだけ早期に行うこととする。
登録はWeb上で行う。
下記の患者データを収集する。
- ステント留置(登録)医療データ
- フォローアップデータ
- 手術(術後退院日まで)
- 死亡
- ステント閉塞/再治療
術前処置BTSとしてステントを留置した患者は手術の後の退院時でフォローアップ終了となる。緩和治療目的の患者フォローアップは留置後12か月で終わる。術前処置BTSとして留置した後に緩和治療目的となった場合にはそのまま12ヶ月のフォローアップをおこなう。
合併症・偶発症や有害事象は診療録に記録するとともに、プロトコールで規定のとおり、通常の偶発症報告書に必要事項を記入して送信する。
本観察研究は、参加医師または参加施設の通常の治療方法を変更することが目的ではない。患者は通常の診療によってフォローアップを受ける。
データはオンラインWeb上で収集される。そして定期的に報告書が発行され提供される。
患者が200例または登録期間終了時まで登録されてフォローアップが12か月に達した後、詳細な最終報告書が研究完了時に発行される。報告された情報を基に出版物が執筆される。
解析を考慮すべきデータ:- 主要評価項目:大腸ステントの臨床的有効性
- 大腸閉塞解除に関する臨床的成功率:臨床的成功症例数/登録数
- 副次的評価項目:技術的成功率および有害事象発生率
- 技術的成功率:ステント留置成功症例数/ステント留置施行数
- 観察期間中の閉塞率および閉塞原因
- 有害事象発生率
- BTSにおける手術への影響(術後合併症発生率、入院期間)
- 生存期間
- その他の評価項目
- 主症状
- 患者および腫瘍の特性
- 留置したステントの種類、および手技ごとのステント数
- 大腸ステント留置前後での大腸閉塞スコア(CROSS)
- 留置後化学療法の有無および内容
- 24時間以内に画像で閉塞の解除を確認できる場合
- 有症状例では症状の低減、
- 無症状で予防的な留置の場合は摂食可能となった場合
- イレウス管挿入例ではステントに変更しても症状の増悪がない場合。
●ステント閉塞は症状の再燃や画像的に口側腸管の拡張が出現した場合や、何らかの再治療を必要とした場合。
ナイチエスTM大腸用ステントは、すでに市販・保険収載されている製品である。
患者データ収集承諾書が作成され、厚生労働省の「個人データ保護に関する指針」に則り、本観察研究について患者に知らせ、その医療データを収集することの承諾を求めるために作られている。患者は通常の診療によって治療を受けるので、その内容は手技への同意を目的とするものではない。
研究責任(分担)医師及び協力者は,研究実施に係る生データ類及び同意書等を取扱う際は,被験者の個人情報保護に十分配慮する。具体的には、施設ごとに識別コード表を作成し,連結可能な匿名化を行う。専用のWeb site上で割付・登録を行い、個人情報(名前,ID番号)が当該施設外へ出ないように留意する。各参加医師に対してPasswordを発行し、セキュリティーに留意する。また,研究の結果を公表する際は,被験者を特定できる情報は排除する。
観察研究であって臨床試験ではないが、各施設の倫理委員会承認は各施設の規定に従う
本研究で使用するデータセンターは下記の通りである。同データセンターは厳重なセキュリティーを行なっており、個人情報保護に十分留意している。今までにいくつかの多施設臨床試験で使用しており、運用や個人情報保護の観点から問題ないと考えられる。
株式会社NTT PCコミュニケーションズ(東京都千代田区神田神保町3-25 住友神保町ビル)のサーバー内にデータセンターを作成。Web上でアクセス可能である。上記サーバー、およびデータベースの管理は株式会社ファースト(東京都渋谷区代々木2−10−4 新宿辻ビル5階・TEL 03-5332-6644・担当者 高橋 雄一)が行う。
本研究は、日本消化器内視鏡学会の附置研究会である「大腸ステント安全手技研究会」を母体として施行され、下記代表が研究責任者である。
連絡先:〒153-8515 東京都目黒区大橋2-17-6 東邦大学医療センター大橋病院 外科内大腸ステント安全手技研究会(Colonic Stent Safe Procedure Research Group)
代表世話人:斉田芳久 事務担当:榎本俊行
電話:03-3468-1251 FAX:03-3469-8506
Name of lead principal investigator:Yoshihisa Saida
Organization: Toho University Ohashi Medical Center
Division name: Department of Surgery
Address: 153-8515 2-17-6 Ohashi Meguro-ku, Tokyo, Japan
また本研究の主たる資金源は、大腸ステント安全手技研究会の研究費であり、その研究費は、日本消化器内視鏡学会からの補助金、各個人会員および賛助会員からの年会費、研究に賛同した企業からの研究寄付金である。
本研究の問い合わせ窓口は、研究内容に関しては前記研究責任研究者に、Web登録に関しては下記研究登録事務局に連絡する。
研究登録事務局責任者:伊佐山浩通
事務:佐々木隆・吉田俊太郎
連絡先:〒113-8655 東京都文京区本郷7-3-1 東京大学 消化器内科
電話:03-3815-5411 FAX:03-3814-0021